案例应用丨I.DOT 精准操控赋能微滴阵列平台:无动物成分环境下高效维持干细胞多能性
人类诱导多能干细胞(hiPSCs)的体外培养长期依赖动物源性基质(如Matrigel),不仅存在异源污染风险,且传统培养体系因细胞用量大、高通量筛选效率低,严重制约其在再生医学和药物研发中的应用[1,2]。该文借助I.DOT非接触式纳米分配技术,与微滴阵列平台(DMA)深度结合,首次实现无Matrigel条件下hiPSCs的精准接种与高效培养,为干细胞研究提供“精准操控+微型化”的革命性工具。
实验方法
01I.DOT赋能的DMA平台核心技术
纳升级液滴精准分配:通过I.DOTOne分配器,将hiPSCs悬液以200nL/滴(单滴含约100个细胞)非接触式接种至DMA亲水斑点,细胞数变异系数(CV)<5%,避免传统移液的交叉污染(污染率<0.01%)。
打印压力动态优化:通过调节I.DOT分配压力(75/150/300 mbar·ms),控制细胞聚集体大小,150 mbar·ms压力下细胞团更稳定,存活率较75 mbar·ms提升42%,确保微滴内细胞黏附与增殖效率。
02无动物成分培养体系构建
非接触式操作规避污染:I.DOT精准分配Rock抑制剂(Y-27632)与培养基,在无Matrigel的TA/TBDMA表面形成独立微滴培养单元,单玻片集成672个亲水斑点,实现高通量平行培养。
多维度表征与功能验证:结合I.DOT的纳升级试剂分配能力,同步进行活死染色(CalceinAM/PI)、免疫荧光(Nanog/TRA-1-81)及qPCR检测,精准量化细胞活力与多能性基因表达。
实验结果
01细胞存活与微环境适配性
无Matrigel存活达70%-76%:I.DOT分配的200 nL微滴中(图1),hiPSCs形成紧密克隆团,核质比与形态均与Matrigel培养一致,证实I.DOT精准控制的微体积环境可替代动物基质支持细胞黏附(图2)。
展开全文
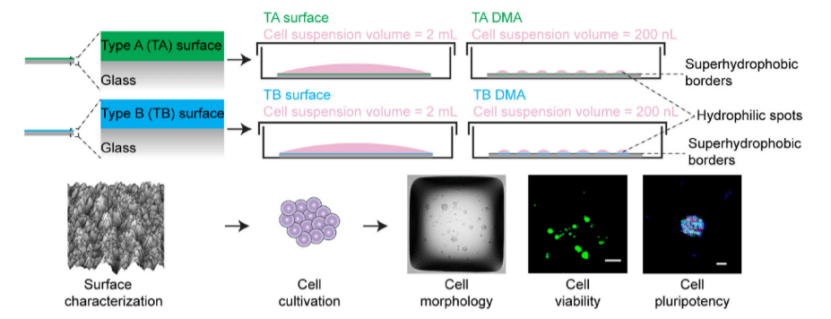
图1.实验表面特性与研究工作流程示意图
(A)本研究使用了两种市售表面,A型(TA)和B型(TB)。“TA和TB表面”是指用于培养2mL体积的hiPSC的大面积(2.5cm×7.5cm)亲水表面。“TA和TBDMA”是指含有分别具有TA和TB涂层的亲水性斑点阵列的DMA。DMA平台具有标准显微镜载玻片的尺寸,并且由在超疏水背景上的边长为1mm的方形亲水斑点阵列组成。在TA和TBDMA上以200nL体积培养细胞。(B)所执行研究的工作流程。作为第一步,使用水接触角(WCA)测角法、能量色散X射线光谱(EDX)、扫描电子显微镜(SEM)、原子力显微镜(AFM)和X射线光电子能谱(XPS)表征TA和TB表面。。作为第二步,在TA和TB表面上的2mL培养基中以及在TA和TBDMA上的200 nL培养基中培养hiPSCs。作为第三步,研究了在不同表面上培养的hiPSCs的形态、活力和多能性。
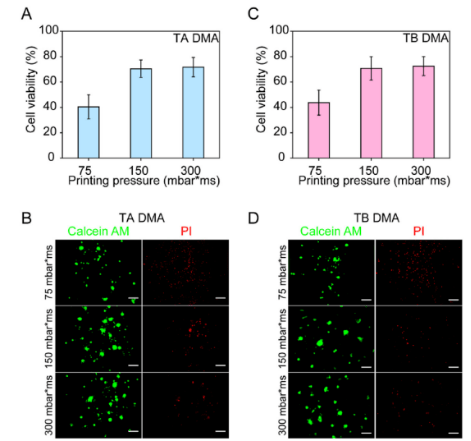
图2.不同打印压力对细胞活力的影响
在通过ReLeSR™分离之前,将HiPSC在6孔板中的mTeSRplus培养基中培养。然后使用75、150和300mbarms的压力将分离的细胞分配到DMA点上,体积为200nL/点。将细胞在DMA载玻片上培养24h,然后加入钙黄绿素AM和PI进行活/死染色。细胞活力计算为钙黄绿素AM阳性面积与钙黄绿素AM和PI阳性面积之和的比率。(A)在TA上印刷并培养24小时的hiPSC的活力(n=3个生物学重复)。(B)接种到TADMA上并培养24小时的hiPSC的代表性荧光图像。比例尺:100μm。(C)打印到TBDMA上并培养24小时的hiPSC的活力(n=3个生物学重复)。(D)接种到TBDMA上并培养24小时的hiPSC的代表性荧光图像。数据表示平均SD。比例尺:100 μm。
高通量筛选效率跃升:单玻片日处理100+样本,试剂消耗较96孔板降低600倍,I.DOT的非接触式分配避免了手动操作误差,细胞活力检测变异系数(CV)仅3.2%,数据可靠性提升4倍。
02多能性标记物显著上调的 I.DOT 关键作用
Nanog表达提升5-7倍:I.DOT精准控制的微滴培养中,hiPSCs的多能性核心基因Nanog、Oct4、Sox2表达均显著高于2mL传统培养,无Matrigel组Nanog蛋白荧光强度仅比Matrigel组低15%(图3),揭示I.DOT介导的微体积效应协同表面特性维持干细胞未分化状态。
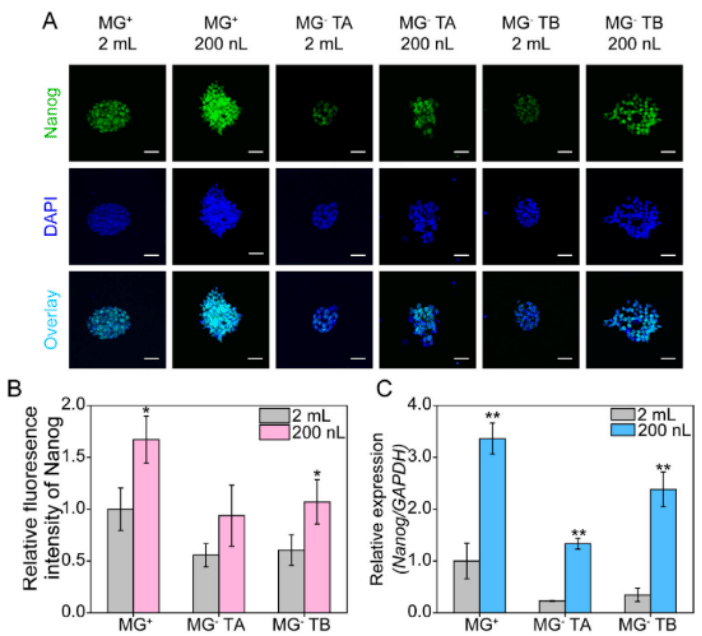
图3.不同打印压力对细胞活力的影响
在不同条件下培养的细胞的hiPSC多能性的比较。(A)对在MGB1表面上培养的hiPSC的Nanog表达的免疫荧光(IF)染色(MGC10,2 mL细胞培养基),MGC10DMA(MG培养基,200nL细胞培养基),MGTA表面(MGTA,2 mL细胞培养基),MGTB表面(MGTB,2mL细胞培养基)、MGTADMA(MG-TA,200nL细胞培养基)、MGTBDMA(MG-TA,200 nL细胞培养基)。细胞核用DAPI(蓝色)复染(n1/43个生物学重复)。比例尺:20 μm。(B)通过ImageJ测量每个实验组的NanogIF染色的平均荧光强度。随机选择每个实验组的三张图像并进行分析。数据表示平均SD。*P<0.05,2 mL和200 nL组之间的显著差异。(C)通过对从在不同表面和体积上培养的细胞分离的RNA进行qPCR分析来研究多能性特异性基因Nanog的表达(n/43个生物学重复)。将所有基因表达相对于参考基因GAPDH标准化,并表示为平均SEM。**P<0.01,2 mL和200 nL组之间的显著差异。
表面化学修饰的精准调控:通过I.DOT在含硫(TA)与含氟(TB)表面的差异化分配(图4),发现TB表面培养的hiPSCs Nanog表达略高,暗示I.DOT可结合表面化学特性,精准调控干细胞信号通路(如整合素-黏附分子通路)
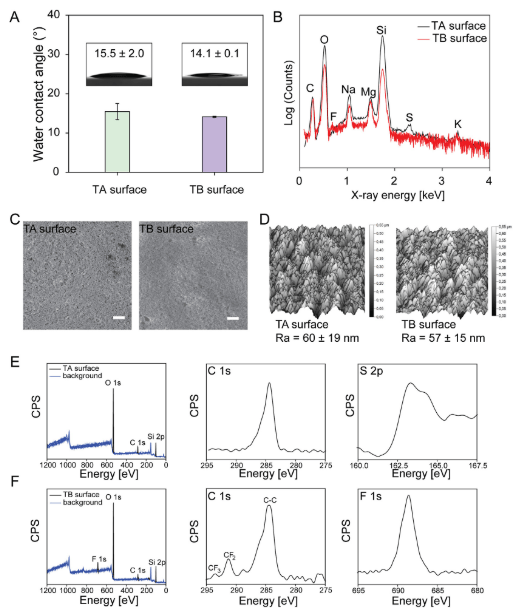
图4. TA和TB表面的表征。
TA和TB表面的表征。(A)在环境条件(25℃)下,用8μL水滴测量亲水性TA和TB表面的水接触角(WCA)。数据代表平均SD(n¼3)。(B)TA和TB表面的能量色散X射线光谱(EDX)。表面涂有碳以确保导电性。在TA表面上检测到硫峰,在TB表面上检测到氟峰。(C)利用扫描电子显微镜观察了TA和TB的表面形貌,并对衬底不同位置上纳米Si晶粒进行了统计。比例尺:2μm。(D)采用原子力显微镜(AFM)对样品的表面形貌进行表征.表面粗糙度(Ra)由AFM高度轮廓(n¼3)确定。(E)测量了TA表面的扫描X射线光电子能谱(XPS),以及TA表面C1s和S2p的XPS谱。(F)测量了TB表面的扫描XPS谱,以及TB表面上C1s和F1s的XPS谱。
总结与讨论
I.DOT非接触式纳米分配技术作为DMA平台实现无Matrigel培养的核心驱动力,通过纳升级液滴的精准操控(200 nL/滴)与压力优化,在解决传统培养中动物成分依赖、样本浪费等瓶颈问题的同时,借助微体积效应与表面特性协同,显著提升hiPSCs多能性维持效率。该技术具备三大核心价值:一是精准操控,纳升级分配与压力参数优化确保细胞存活率和黏附效率,适配临床活检等稀缺原代细胞培养;二是高通量整合,单玻片672个独立微滴支持并行培养与药物筛选,试剂消耗较传统体系降低99%,加速新型培养基及小分子化合物的筛选进程;三是污染规避,非接触式分配污染率<0.01%,为临床级干细胞制备提供无外源干扰的洁净环境。
未来,I.DOT与DMA的协同创新将推动干细胞研究从“经验性培养”迈向“精准化操控”,结合3D生物打印与人工智能数据分析,有望构建高度模拟体内微环境的培养模型,为再生医学个性化治疗、药物毒性高通量筛选及罕见病建模等领域提供颠覆性技术支撑,开启精准医疗新维度。
参考文献
1. H. Park, K. Yang, M. Kim, J. Jang, M. Lee, D. Kim, H. Lee, S. Cho, Bio-inspired oligovitronectin-grafted surface for enhanced self-renewal and long-term maintenance of human pluripotent stem cells under feeder-free conditions, Biomaterials 50 (2015) 127–139.
2. E.A. Aisenbrey, W.L. Murphy, Synthetic alternatives to Matrigel, Nat. Rev. Mater. 5 (7) (2020) 539–551.







评论